중남미
"
"
의료기기
화장품
ANVISA(의료기기)
ANVISA (브라질식의약품감시국) : 브라질 보건복지부 산하의 의료기기, 의약품 및 화장품 등 허가 및 감시기관
Food, Cosmetics, Sanitizing Products, Tabacco, Toxicology(Pesticides), Halth Services, Drugs, Medical Devices, Laboratorles, Blood and blood Products, Post-market Survaillance, Marketing Control, Ports, airports and Frontiers, International, Market Regulation
등록절차 순서도
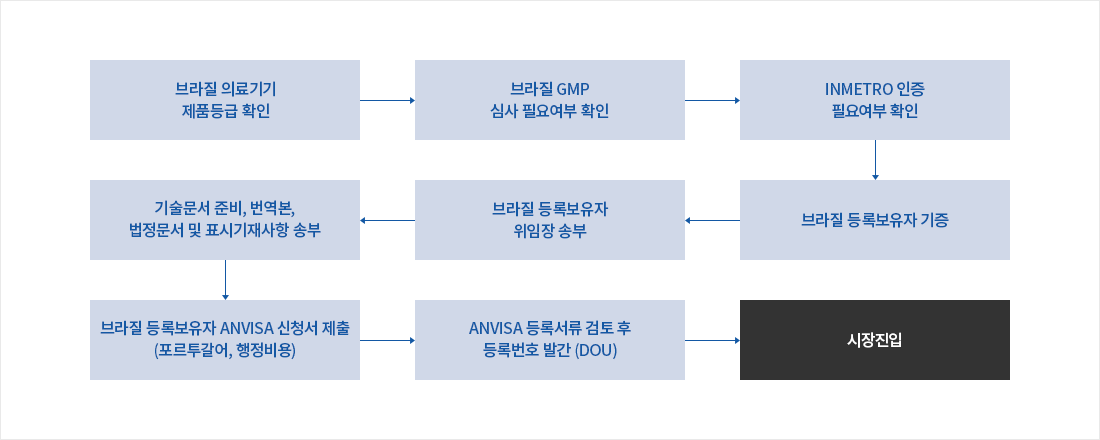
- 1. 브라질 의료기기 제품등급 확인
- 2. 브라질 GMP 심사 필요여부 확인
- 3. INMETRO 인증 필요여부 확인
- 4. 브라질 등록보유자 기증
- 5. 브라질 등록보유자 위임장 송부
- 6. 기술문서 준비, 번역본, 법정문서 및 표시기재사항 송부
- 7. 브라질 등록보유자 ANVISA 신청서 제출(포르투갈어, 행정비용)
- 8. ANVISA 등록서류 검토 후 등록번호 발간(DOU)
- 9. 시장진입
브라질 의료기기 등급 분류
유럽 CE 및 한국의료기기 등급분류 체계와 유사하며 인체에 대한 잠재적 위험성에 따라 분류
| 분류 | 예시 | 등록방법 | |
|---|---|---|---|
| I | Low Risk | 대부분의 비 침습 제품 | 약식등록 (Cadastro) |
| II | Medium Risk | 비 침습제품 중 혈액 보관용기, 단기접촉 침습제품 및 진단장치 |
약식등록/등록 (Cadastro/Registro) |
| III | High Risk | 대부분의 침습제품 및 대부분의 전기제품 | 중독 (Registro) |
| IV | Maximum Risk | 대부분의 이식제출 주료장기 관련 제품 | 중독 (Registro) |
INMETRO 인증
- - 전기사용 의료장비, 주사침, 주사기, 혈액용기, 일부 측정장비 및 인공유방 등에 필수 적용
- - INMETRO 인정기관에 의해 인증절차 (시험 및 심사) 수행
- - ILAC 시험기관 시험결과 인증 (2년이내)
- - 5년 유효기간 및 매년 갱신 필수
브라질 GMP
- - ISO 13485 및 한국 GMP 법령과 유사
- - 3, 4 등급의 의료기기 제조소 GMP 심사 필수
- - 1, 2등급의 경우 필수는 아니며 INMETRO 인증만 진행
- - 5년 유효기간 (만료 12개월 전에 재등록 필수)
브라질 등록 보유자 (BRH, Brazilian Registration Holder)
- - 브라질 역내에 지사가 없는 경우 필수적으로 지정
- - 브라질 등록권에 대한 법적 소유자이며, 제조자의 제품을 위해서 ANVISA와 커뮤니케이션을 담당
KTR 지원분야
- - ANVISA 업무 지원 및 최신 규제 동향 제공
- - 브라질 의료기기 등급 확인
- - INMETRO 인증필요 여부 확인 및 인증지원
- - 적절한 브라질 내 파트너 발굴 및 최적의 진출 전략 제공
- · 컨설팅 기업
- · BRH
- · 수입자 및 유통업자
- - 기타 컨설팅 제공
글로벌전략실
E-mail : gmhelp@ktr.or.kr
Tel : 02-2164-1498



